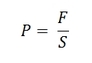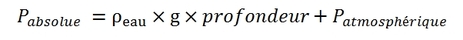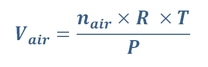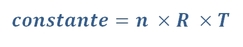Partie 1 - La pression, définitions et lois
Avant de pouvoir étudier les effets de la pression* sur l'apnéiste, nous expliquons dans cette première partie quelques définitions et lois se rapportant au phénomène de pression pour pouvoir comprendre les parties suivantes.
- La pression est la force pressante F exercée par un fluide (liquide ou gaz) et exprimée en Newton* sur une surface S en m². La pression P est ainsi donnée par la formule :
Elle s’exprime donc en Newton par mètre carré, ou plus simplement en Pascal*. En plongée sous-marine, on l’exprime en bar*, 1 bar étant égal à 100 000 Pa, ou plus simplement à 1000 hPa.
Il faut bien distinguer les différents types de pressions :
- la pression atmosphérique* : c’est la pression de l’air qui nous entoure. Cette pression diminue avec l’altitude. A altitude 0, elle est en moyenne de 1013,25 hPa, soit 1,01325 bar ; pour simplifier nous arrondissons à 1 bar.
- la pression hydrostatique* : c’est la pression exercée par l’eau. Nous avons procédé à une expérience pour déterminer la relation entre pression et profondeur.
Expérience 1 : relation entre pression et profondeur
(cliquez sur la photo pour accéder directement au compte rendu détaillé)
Il faut bien distinguer les différents types de pressions :
- la pression atmosphérique* : c’est la pression de l’air qui nous entoure. Cette pression diminue avec l’altitude. A altitude 0, elle est en moyenne de 1013,25 hPa, soit 1,01325 bar ; pour simplifier nous arrondissons à 1 bar.
- la pression hydrostatique* : c’est la pression exercée par l’eau. Nous avons procédé à une expérience pour déterminer la relation entre pression et profondeur.
Expérience 1 : relation entre pression et profondeur
(cliquez sur la photo pour accéder directement au compte rendu détaillé)
Nous avons conclu de cette expérience que la pression augmente proportionnellement avec la profondeur.
On a ensuite déduit la formule suivante :
On a ensuite déduit la formule suivante :
Avec :
- masse volumique de l’eau ρeau= 1000 kg.m-3
- intensité de la pesanteur terrestre g = 9.8 N.kg-1
- profondeur en mètres
- pression atmosphérique en Pascal
Enfin, nous avons calculé avec cette formule que tous les 10 mètres de profondeur, la pression augmente à raison de 1 bar environ.
- la pression absolue* : c’est l’addition de la pression atmosphérique et hydrostatique.
On a ainsi la formule suivante :
- masse volumique de l’eau ρeau= 1000 kg.m-3
- intensité de la pesanteur terrestre g = 9.8 N.kg-1
- profondeur en mètres
- pression atmosphérique en Pascal
Enfin, nous avons calculé avec cette formule que tous les 10 mètres de profondeur, la pression augmente à raison de 1 bar environ.
- la pression absolue* : c’est l’addition de la pression atmosphérique et hydrostatique.
On a ainsi la formule suivante :
Avec :
- masse volumique de l’eau ρeau = 1000 kg.m-3
- intensité de la pesanteur terrestre g = 9.8 N.kg-1
- profondeur en mètres
- pression absolue et atmosphérique en Pascal
Ainsi, quand un apnéiste plonge à 100m de profondeur, la pression s’exerçant sur lui est de 1 bar (pression atmosphérique) + 10 bars (pression hydrostatique) = 11 bars, soit 11 fois plus que la pression éprouvée par l’apnéiste à la surface.
- masse volumique de l’eau ρeau = 1000 kg.m-3
- intensité de la pesanteur terrestre g = 9.8 N.kg-1
- profondeur en mètres
- pression absolue et atmosphérique en Pascal
Ainsi, quand un apnéiste plonge à 100m de profondeur, la pression s’exerçant sur lui est de 1 bar (pression atmosphérique) + 10 bars (pression hydrostatique) = 11 bars, soit 11 fois plus que la pression éprouvée par l’apnéiste à la surface.
- La loi de Boyle et Mariotte a été découverte à la fin du 17ème siècle. Elle énonce qu’à température constante, lors de l'augmentation de pression d'un gaz, son volume diminue et inversement. Afin de prouver cette loi et d’en déduire une formule physique, nous avons procédé à une première expérience.
Expérience 2 : preuve de la loi de Boyle-Mariotte
(cliquez sur la photo pour accéder directement au compte rendu détaillé)
Nous avons conclu de cette expérience que la pression augmente proportionnellement avec l’inverse du volume d’un gaz.
On a ensuite déduit la formule suivante :
On a ensuite déduit la formule suivante :
C’est-à-dire :
Avec :
- volume V en litres
- pression P en Pascal
- constante qui dépend de la température et de la quantité de matière de gaz
Ainsi, quand la pression exercée sur un gaz augmente, son volume diminue proportionnellement, et inversement : c’est la loi de Boyle-Mariotte. Cette loi est vraie pour tous les gaz. On peut expliquer cette proportionnalité en se plaçant à l’échelle macroscopique : quand la pression baisse, les molécules formant un gaz s’éloignent les unes des autres, augmentant ainsi le volume occupé par le gaz. Cependant, cette loi n’est applicable qu’à température constante, et pour des faibles pressions.
Pour aller plus loin :
(Tous les raisonnements et calculs sont précisés dans l’onglet Expérience 2)
En vérifiant la loi des gaz parfaits avec les données de notre expérience, on découvre que si on suppose que l’air est un mélange de gaz parfaits, on a la formule suivante :
- volume V en litres
- pression P en Pascal
- constante qui dépend de la température et de la quantité de matière de gaz
Ainsi, quand la pression exercée sur un gaz augmente, son volume diminue proportionnellement, et inversement : c’est la loi de Boyle-Mariotte. Cette loi est vraie pour tous les gaz. On peut expliquer cette proportionnalité en se plaçant à l’échelle macroscopique : quand la pression baisse, les molécules formant un gaz s’éloignent les unes des autres, augmentant ainsi le volume occupé par le gaz. Cependant, cette loi n’est applicable qu’à température constante, et pour des faibles pressions.
Pour aller plus loin :
(Tous les raisonnements et calculs sont précisés dans l’onglet Expérience 2)
En vérifiant la loi des gaz parfaits avec les données de notre expérience, on découvre que si on suppose que l’air est un mélange de gaz parfaits, on a la formule suivante :
Avec :
- volume du gaz Vair en m3
- pression P en pascal
- quantité de matière d’air nair en moles
- constante des gaz parfaits R = 8.314 Pa.m3.K-1.mol-1
- température T en Kelvin (= T (°C) + 273.15)
Par conséquent, dans des conditions normales de pression et de températures, pour des gaz supposés parfaits, on a :
- volume du gaz Vair en m3
- pression P en pascal
- quantité de matière d’air nair en moles
- constante des gaz parfaits R = 8.314 Pa.m3.K-1.mol-1
- température T en Kelvin (= T (°C) + 273.15)
Par conséquent, dans des conditions normales de pression et de températures, pour des gaz supposés parfaits, on a :
Afin de démontrer en pratique la loi de Boyle-Mariotte, nous avons effectué une autre expérience.
Expérience 3 : application de la loi de Boyle-Mariotte
(cliquez sur la photo pour accéder directement au compte rendu détaillé)
On a pu conclure de cette expérience que le volume d’un gaz augmente quand la pression baisse (c’est-à-dire que le diamètre d’un ballon augmente quand il est amené en altitude), et qu’il diminue quand la pression augmente (c’est-à-dire que le diamètre d’un ballon diminue quand il est ramené à une altitude plus faible).
On a donc vérifié la loi de Boyle-Mariotte, et par conséquent, puisqu’on a aussi prouvé que la pression augmente avec la profondeur, on peut en conclure que plus l’apnéiste plonge profondément, plus l’air contenu dans son corps va voir son volume diminuer.
Schéma de la diminution du volume d'un ballon avec l’augmentation de la profondeur
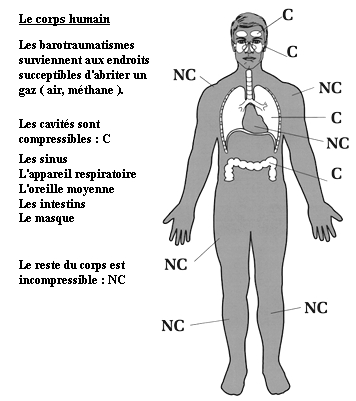
L’augmentation de la pression n’a d’effets que sur les parties du corps contenant de l’air, car la pression n’a d’effet que sur les gaz. Le schéma ci-dessus présente ces différentes cavités*.