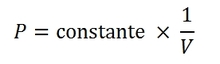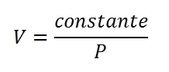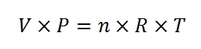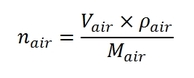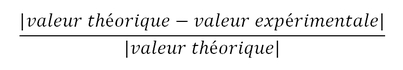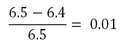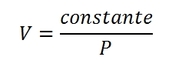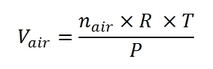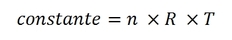Expérience 2
Nous avons réalisé cette expérience pour prouver et déduire une formule physique de la loi de Boyle-Mariotte qui énonce qu’à température constante, lors de l'augmentation de pression d'un gaz, son volume diminue et inversement.
- Matériels :
- Vue d'ensemble du dispositif expérimental :
- Protocole :
Nous emprisonnons 60 cm3 d’air dans la seringue, puis diminuons le volume contenu dans la seringue, jusqu’à 30 cm3, tout en notant à chaque 5 cm3 de volume soustrait la pression régnant dans la seringue grâce au manomètre.
- Tableaux récapitulatifs des résultats :
Pour plus de précision, on ajoute aux volumes d’air contenus dans la seringue le volume d’air contenu dans le tube, c’est-à-dire 4 cm3.
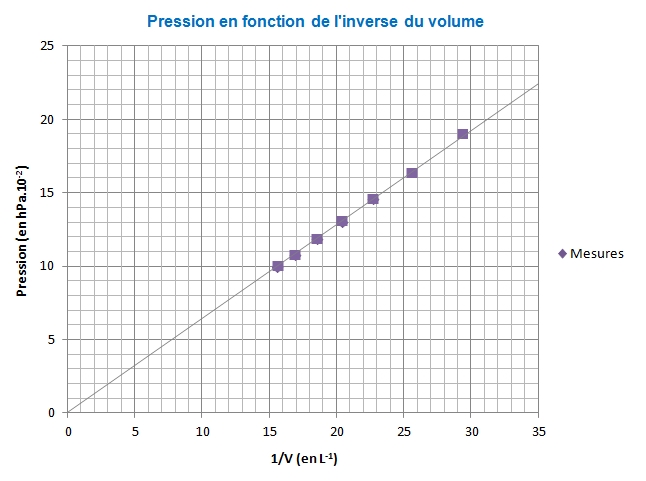
- Expression des résultats sous forme de graphique :
- Conclusion de l’expérience :
Nous avons pu observer que plus on réduit le volume d’air à l’intérieur de la seringue, plus la pression à l’intérieur de la seringue augmente.
Grâce au graphique, on découvre que les points exprimant les sept pressions mesurées en fonction de l’inverse des différents volumes forment une droite alignée avec l’origine. On peut en conclure qu’il y a proportionnalité entre pression et volume d’un gaz.
Nous avons déterminé le coefficient de proportionnalité de cette relation: il est d’environ 0.6429 hPa.10-2/L, soit 6.429 ×103 Pa/L.
On a ainsi la fonction linéaire suivante (l’ordonnée à l’origine étant nulle) :
C’est-à-dire :
Avec :
- volume V en litres
- pression P en Pascal
- constante = 6.429 ×10-3 Pa/L, mais uniquement dans le cas de notre expérience : cette constante peut varier, elle dépend de la température et de la quantité de matière de gaz
Ainsi, quand la pression exercée sur un gaz augmente, son volume diminue proportionnellement, et inversement : c’est la loi de Boyle-Mariotte. Cette loi est vraie pour tous les gaz. On peut expliquer cette proportionnalité en se plaçant à l’échelle macroscopique : quand la pression baisse, les molécules formant un gaz s’éloignent les unes des autres, augmentant ainsi le volume occupé par le gaz. Cependant, cette loi n’est applicable qu’à température constante, et pour des faibles pressions.
Pour aller un peu plus loin…
Le gaz parfait est un modèle simplifié des gaz réels, énoncé au 18ème siècle, et décrivant le comportement des gaz à basse pression. Selon ce modèle, les molécules formant un gaz se comportent comme des sphères rebondissant les unes contre les autres, elles peuvent donc se percuter ; cependant, ce modèle ne tient pas compte des interactions des molécules autres que celles ayant lieu au moment des chocs, ni du volume propre des molécules devant le volume occupé par le gaz.
En théorie, tous les types de gaz vérifient ce modèle aux conditions normales de température et de pression, c’est-à-dire à 0°C et à la pression atmosphérique moyenne de 1013.25 hPa. En pratique, un gaz parfait n’existe pas, mais des gaz réels peuvent se comporter globalement comme le modèle du gaz parfait, à une pression faible.
La loi des gaz parfaits est la suivante :
- volume V en litres
- pression P en Pascal
- constante = 6.429 ×10-3 Pa/L, mais uniquement dans le cas de notre expérience : cette constante peut varier, elle dépend de la température et de la quantité de matière de gaz
Ainsi, quand la pression exercée sur un gaz augmente, son volume diminue proportionnellement, et inversement : c’est la loi de Boyle-Mariotte. Cette loi est vraie pour tous les gaz. On peut expliquer cette proportionnalité en se plaçant à l’échelle macroscopique : quand la pression baisse, les molécules formant un gaz s’éloignent les unes des autres, augmentant ainsi le volume occupé par le gaz. Cependant, cette loi n’est applicable qu’à température constante, et pour des faibles pressions.
Pour aller un peu plus loin…
Le gaz parfait est un modèle simplifié des gaz réels, énoncé au 18ème siècle, et décrivant le comportement des gaz à basse pression. Selon ce modèle, les molécules formant un gaz se comportent comme des sphères rebondissant les unes contre les autres, elles peuvent donc se percuter ; cependant, ce modèle ne tient pas compte des interactions des molécules autres que celles ayant lieu au moment des chocs, ni du volume propre des molécules devant le volume occupé par le gaz.
En théorie, tous les types de gaz vérifient ce modèle aux conditions normales de température et de pression, c’est-à-dire à 0°C et à la pression atmosphérique moyenne de 1013.25 hPa. En pratique, un gaz parfait n’existe pas, mais des gaz réels peuvent se comporter globalement comme le modèle du gaz parfait, à une pression faible.
La loi des gaz parfaits est la suivante :
Avec :
- volume du gaz V en m3
- pression P en pascal
- quantité de matière de gaz n en moles
- constante des gaz parfaits R = 8.314 Pa.m3.K-1.mol-1
- température T en Kelvin (= T (°C) + 273.15)
L’air est principalement composé de dioxygène et d’azote ; si l’on considère que notre expérience s’est déroulée dans les conditions normales de températures et de pression, on peut essayer d’appliquer la formule des gaz parfaits à notre expérience.
Prenons comme données la première de nos mesures.
Données :
- Vair = 64 cm3 = 6.4E-5 m3
- P = 1003 hPa = 1.003E 5 Pa
Donc : valeur expérimental Vair × P = 6.4 m3.Pa
Données :
- R = 8.314 Pa.m3.K-1.mol-1
- T = 20°C + 273.15 = 293.15 K
- nair : on admet la formule suivante :
- volume du gaz V en m3
- pression P en pascal
- quantité de matière de gaz n en moles
- constante des gaz parfaits R = 8.314 Pa.m3.K-1.mol-1
- température T en Kelvin (= T (°C) + 273.15)
L’air est principalement composé de dioxygène et d’azote ; si l’on considère que notre expérience s’est déroulée dans les conditions normales de températures et de pression, on peut essayer d’appliquer la formule des gaz parfaits à notre expérience.
Prenons comme données la première de nos mesures.
- Cherchons la valeur expérimentale Vair × P grâce aux données de l’expérience.
Données :
- Vair = 64 cm3 = 6.4E-5 m3
- P = 1003 hPa = 1.003E 5 Pa
Donc : valeur expérimental Vair × P = 6.4 m3.Pa
- Cherchons maintenant la valeur théorique Vair × P avec la formule des gaz parfaits.
Données :
- R = 8.314 Pa.m3.K-1.mol-1
- T = 20°C + 273.15 = 293.15 K
- nair : on admet la formule suivante :
Avec :
- la quantité de matière cherchée nair en moles
- le volume d’air Vair en litres = 64 cm3 = 6.4E-2 L
- la masse volumique de l’air ρair en g/L = 1,2 kg/m3 = 1.2 g/L
- la masse molaire de l’air Mair en g/mol :
L’air étant composé à 78% de diazote N2 et à 22% de dioxygène O2, on a :
Mair = 0.78 × M(N2) + 0.22 × M(O2) = 0.78 × 28.0 + 0.22 × 32.0 = 28.9 g/mol
Application numérique :
nair = (6.4E-2 × 1.2) / 28.9 = 2.7 moles
Ecriture littérale :
Vair × P = nair × R × T
Application numérique :
Vair × P = 2.7× 8.314 × 293.15 = 6.5 m3.Pa
Donc : valeur théorique Vair × P = 6.5 m3.Pa
- la quantité de matière cherchée nair en moles
- le volume d’air Vair en litres = 64 cm3 = 6.4E-2 L
- la masse volumique de l’air ρair en g/L = 1,2 kg/m3 = 1.2 g/L
- la masse molaire de l’air Mair en g/mol :
L’air étant composé à 78% de diazote N2 et à 22% de dioxygène O2, on a :
Mair = 0.78 × M(N2) + 0.22 × M(O2) = 0.78 × 28.0 + 0.22 × 32.0 = 28.9 g/mol
Application numérique :
nair = (6.4E-2 × 1.2) / 28.9 = 2.7 moles
Ecriture littérale :
Vair × P = nair × R × T
Application numérique :
Vair × P = 2.7× 8.314 × 293.15 = 6.5 m3.Pa
Donc : valeur théorique Vair × P = 6.5 m3.Pa
- Incertitude relative entre valeur théorique et valeur expérimentale :
Application numérique :
On a donc une incertitude relative inférieure à 10%, c’est-à-dire inférieure à 0.1.
Conclusion :
Nous avions abouti grâce aux données de notre expérience à la formule suivante :
Conclusion :
Nous avions abouti grâce aux données de notre expérience à la formule suivante :
Mais en vérifiant la loi des gaz parfaits avec des données de notre expérience, on découvre que si on suppose que l’air est un mélange de gaz parfaits, on a la formule suivante :
Avec :
- volume du gaz Vair en m3
- pression P en pascal
- quantité de matière d’air nair en moles
- constante des gaz parfaits R = 8.314 Pa.m3.K-1.mol-1
- température T en Kelvin (= T (°C) + 273.15)
Par conséquent, dans des conditions normales de pression et de températures, pour des gaz supposés parfaits, on a :
- volume du gaz Vair en m3
- pression P en pascal
- quantité de matière d’air nair en moles
- constante des gaz parfaits R = 8.314 Pa.m3.K-1.mol-1
- température T en Kelvin (= T (°C) + 273.15)
Par conséquent, dans des conditions normales de pression et de températures, pour des gaz supposés parfaits, on a :